
-
中文 | EN

中文 | EN
发布时间:2023-07-05 00:00:00.0
氧气浓度对于维持机体稳态起到了非常重要的作用,长时间的低氧压力会造成很多疾病,比如中风,心血管疾病和炎症性肠病等。机体在低氧条件下可通过抑制EglN1/pVHL通路来诱导HIFα蛋白水平的增加,从而启动HIFα下游通路,保护机体的能量代谢稳态。但是当细胞不能承受这种低氧压力的时候,细胞就会发生死亡。然而,目前低缺氧促进细胞死亡的分子机制仍不清楚, 同时,氧气的感受蛋白EglN1/pVHL在正常条件下促进细胞成活的机理有待进一步阐明。
2023年7月3日,中国科学院生物与化学交叉研究中心袁钧瑛课题组,许代超课题组,和美国哈佛医学院的魏文毅课题组合作在Nature Cell Biology上发表了题为Prolonged hypoxia alleviates prolyl hydroxylation-mediated suppression of RIPK1 to promote necroptosis and inflammation的文章,解析了低氧诱导RIPK1介导的细胞程序性坏死和炎症的分子机制。

文章作者发现在短时间或者轻度低氧的条件下,细胞会激活HIFα通路来适应低氧条件,而在长时间或者过度低氧的条件下会激活RIPK1, 进而促进下游细胞程序性坏死和炎症的发生。机制上,作者发现低氧主要通过降低RIPK1在体内的羟基化水平来诱导细胞程序性坏死的发生。文章证明了羟基化酶EgLN1可以羟基化RIPK1,而羟基化后的RIPK1通过招募pVHL蛋白和RIPK1的酶活区域结合,进而进一步阻断RIPK1的活化(图1)。而且缺氧对RIPK1激酶活性的调控并不是通过之前发现的TNFα/TNFR1通路来实现的。
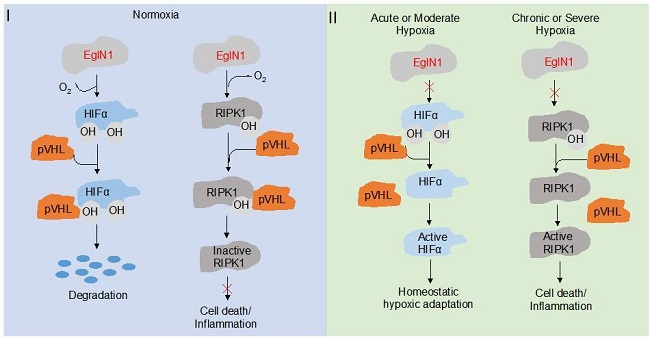
图1:低氧激活RIPK1介导的细胞程序性坏死的分子机制
首先,作者通过体内和体外实验验证了缺氧能够激活RIPK1所依赖的细胞死亡和炎症的发生。接着作者发现RIPK1体内被羟基化酶EGLNs在P195位点上发生羟基化修饰。为了进一步证明羟基化酶对RIPK1活性的调控作用,文章作者体内和体外敲除羟基化酶或者用羟基化酶的小分子抑制剂FG-4592 处理细胞和小鼠,发现羟基化修饰RIPK1是抑制其激酶活性,从而抑制了细胞死亡和炎症的发生。而羟基化的RIPK1通过招募pVHL的结合进一步抑制了RIPK1的活性。为了探究RIPK1和pVHL的结合模式,文章作者通过共结晶的方法解析了羟基化的RIPK1小肽和pVHL所形成的复合物结构。最后作者通过肝脏特异性敲除VHL来研究VHL在体内对RIPK1激酶活性的调控。文章作者发现肝脏敲出VHL 可以激活RIPK1和RIPK1所依赖的细胞死亡和炎症。更重要的是,作者发现抑制RIPK1的激酶活性可以大大延长VHL敲除小鼠的寿命。
该研究阐明了低氧条件下细胞激活RIPK1从而诱导程序性坏死发生的分子机制,揭示了氧气感受器蛋白EglN1/pVHL控制细胞存活的重要机理,同时该研究提示抑制RIPK1激酶活性能够为治疗中风、低氧性炎症和神经退行疾病等疾病提供新的理论基础和新的治疗方案。
该工作受到了国家重点研发计划,国家自然科学基金委,中科院先导专项,和上海市科委的资助。
原文链接:https://www.nature.com/articles/s41556-023-01170-4
